Trang chủ » Nghiên cứu » Hệ bạch huyết và hạch canh gác: đường dẫn ung thư di căn
Hệ bạch huyết và hạch canh gác: đường dẫn ung thư di căn
- Xuất bản trực tuyến Ngày 15 tháng 10 năm 2021
- Tác giả: Stanley P. Leong , 1, 8 Alexander Pissas , 2 Muriel Scarato , 2 Francoise Gallon , 2 Marie Helene Pissas , 2 Miguel Amore , 3, 4 Max Wu , 5 Mark B. Faries , 6 và Amanda W. Lund 7

- Link nghiên cứu: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8967769/
Các từ viết tắt
Nội dung chính
| SLN | Hạch bạch huyết |
| CT | Chụp cắt lớp vi tính |
| CHÚNG TA | Siêu âm |
| MRI | Chụp cộng hưởng từ |
| THÚ CƯNG | Chụp cắt lớp phát xạ positron |
| DC | Tế bào đuôi gai |
| VEGF-C | Yếu tố tăng trưởng nội mô mạch máu |
Tổng quan
- Bệnh tự kỷ, giảm trí nhớ và sương mù não: Thải độc Hệ bạch huyết vùng đầu như thế nào?
- Hệ thống bạch huyết: Đánh giá về tác động của nắn chỉnh xương
- Lập bản đồ hệ thống bạch huyết trên các quy mô cơ thể và các lĩnh vực chuyên môn: Báo cáo từ hội thảo của Viện Tim, Phổi và Máu Quốc gia năm 2021 tại Hội nghị chuyên đề về bạch huyết Boston
- Cấu trúc và sinh lý mạng lưới mạch bạch huyết – Phần 8: Bạch huyết đường liêu hóa và liệu pháp miễn dịch
- Cấu trúc và sinh lý mạng lưới mạch bạch huyết – Phần 7: Phù bạch huyết
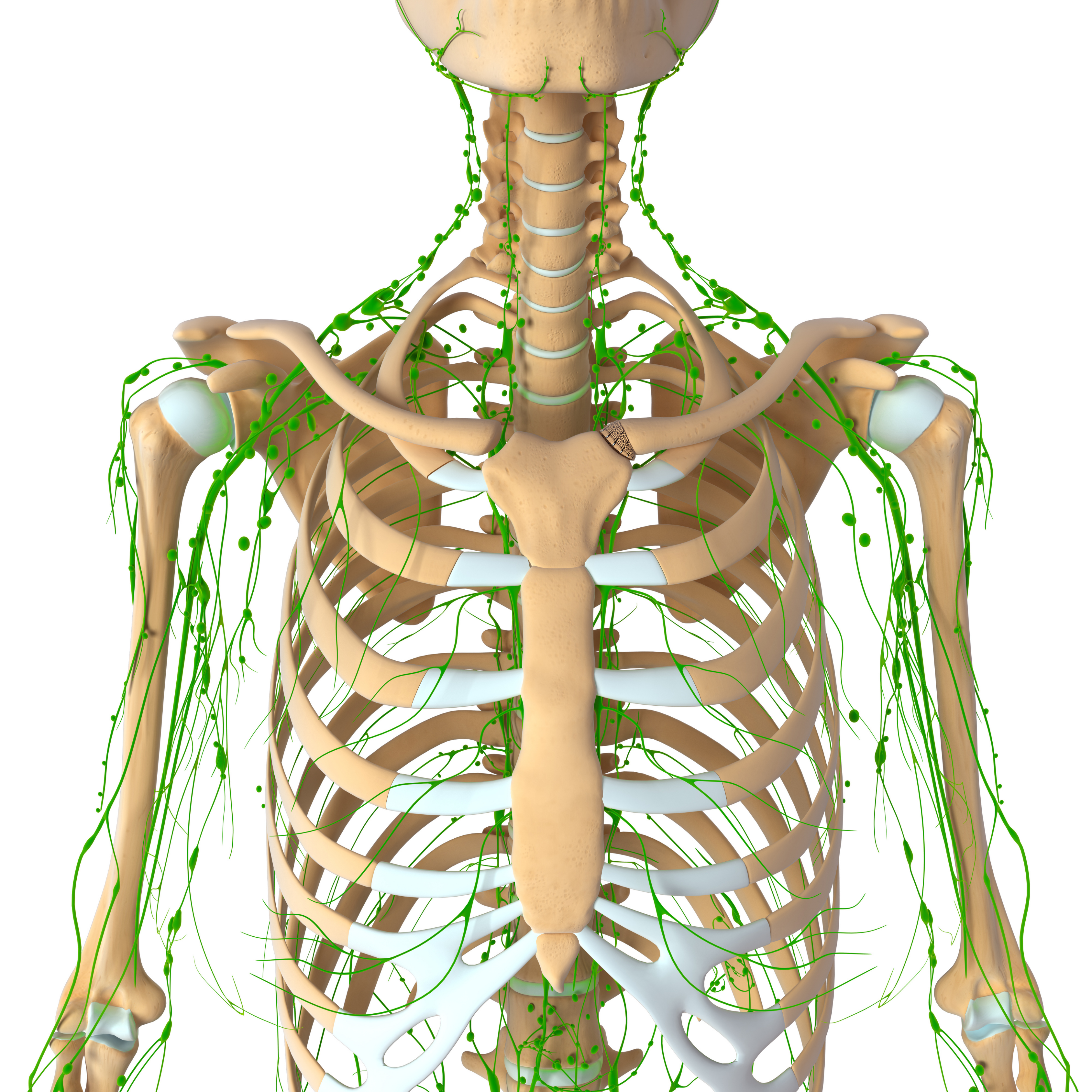
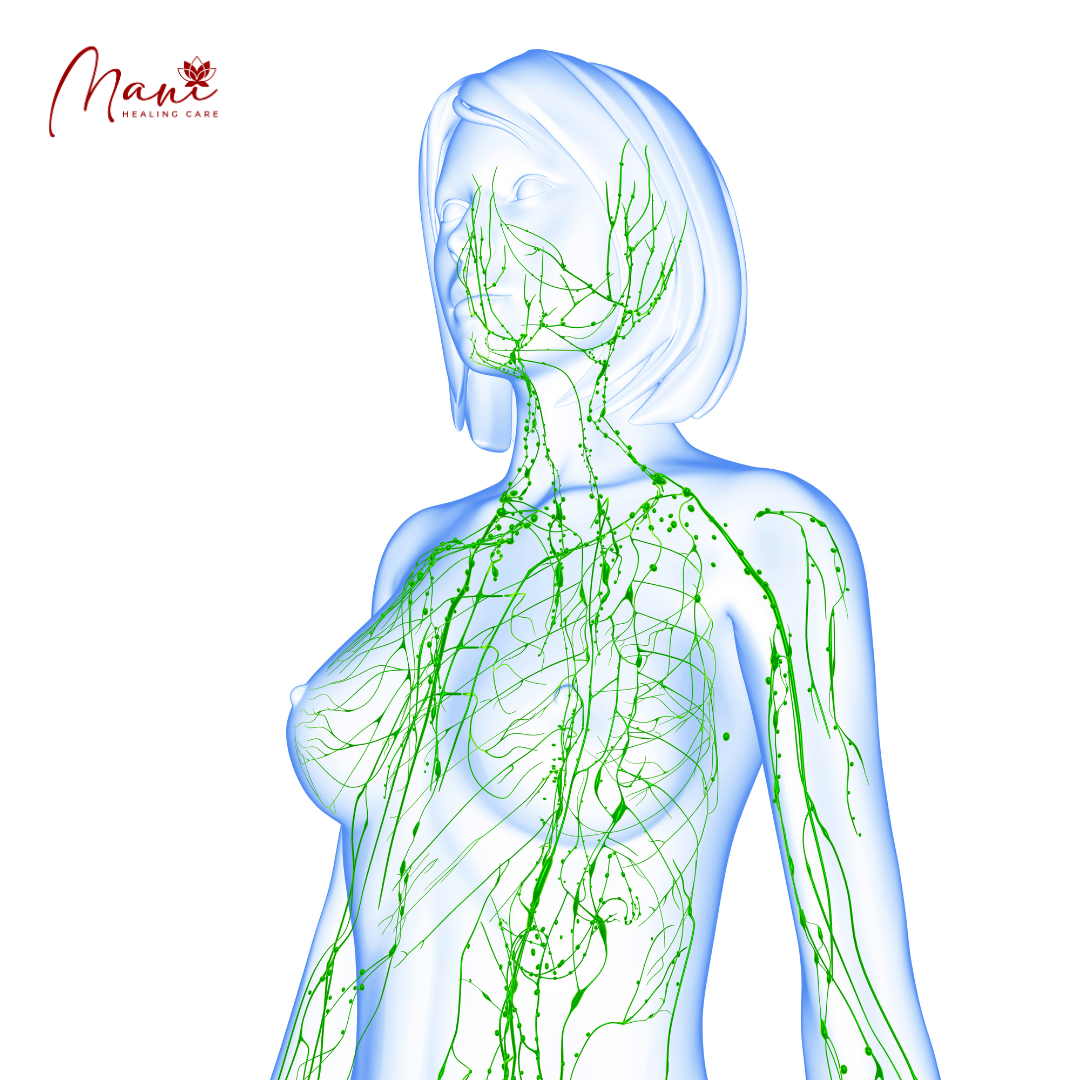
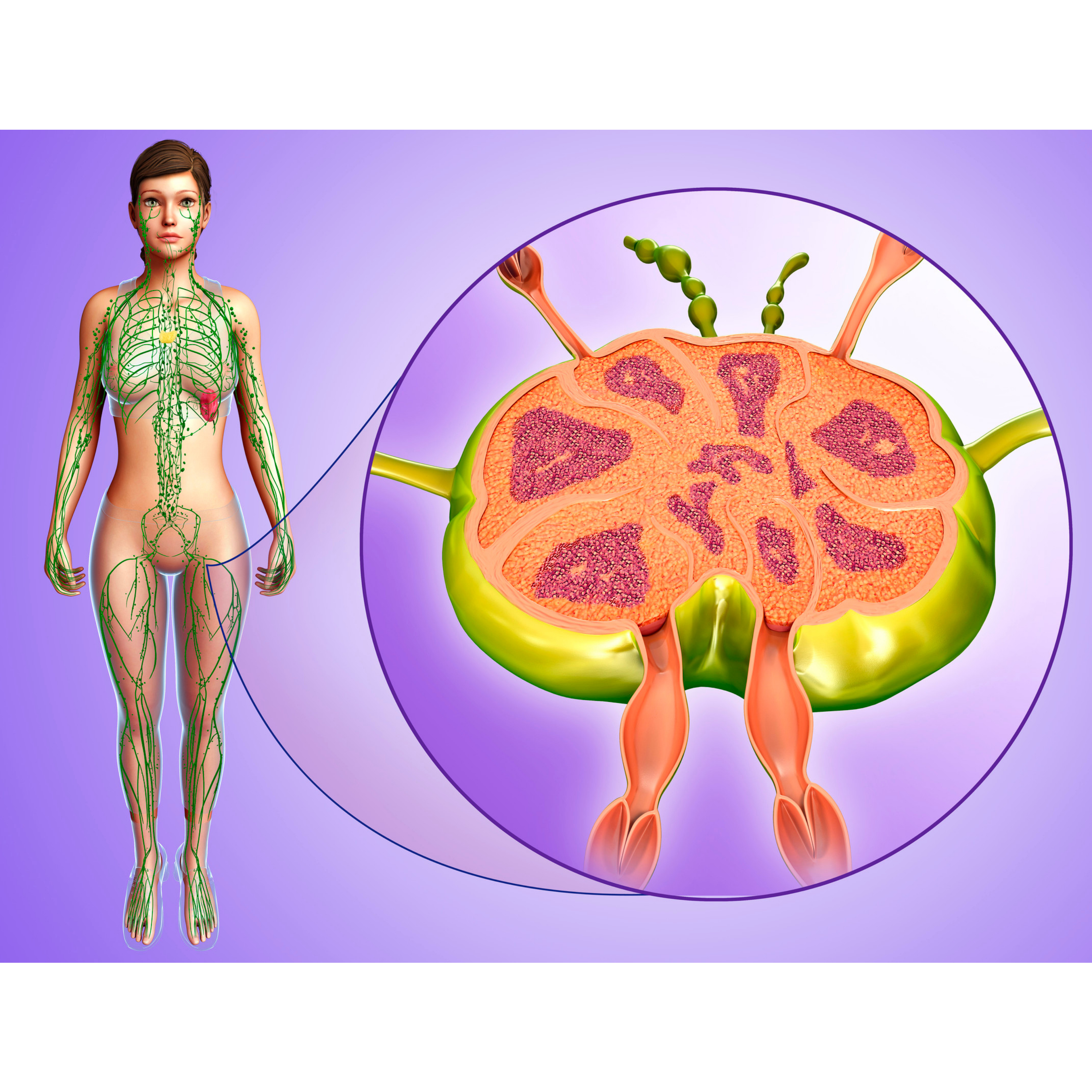
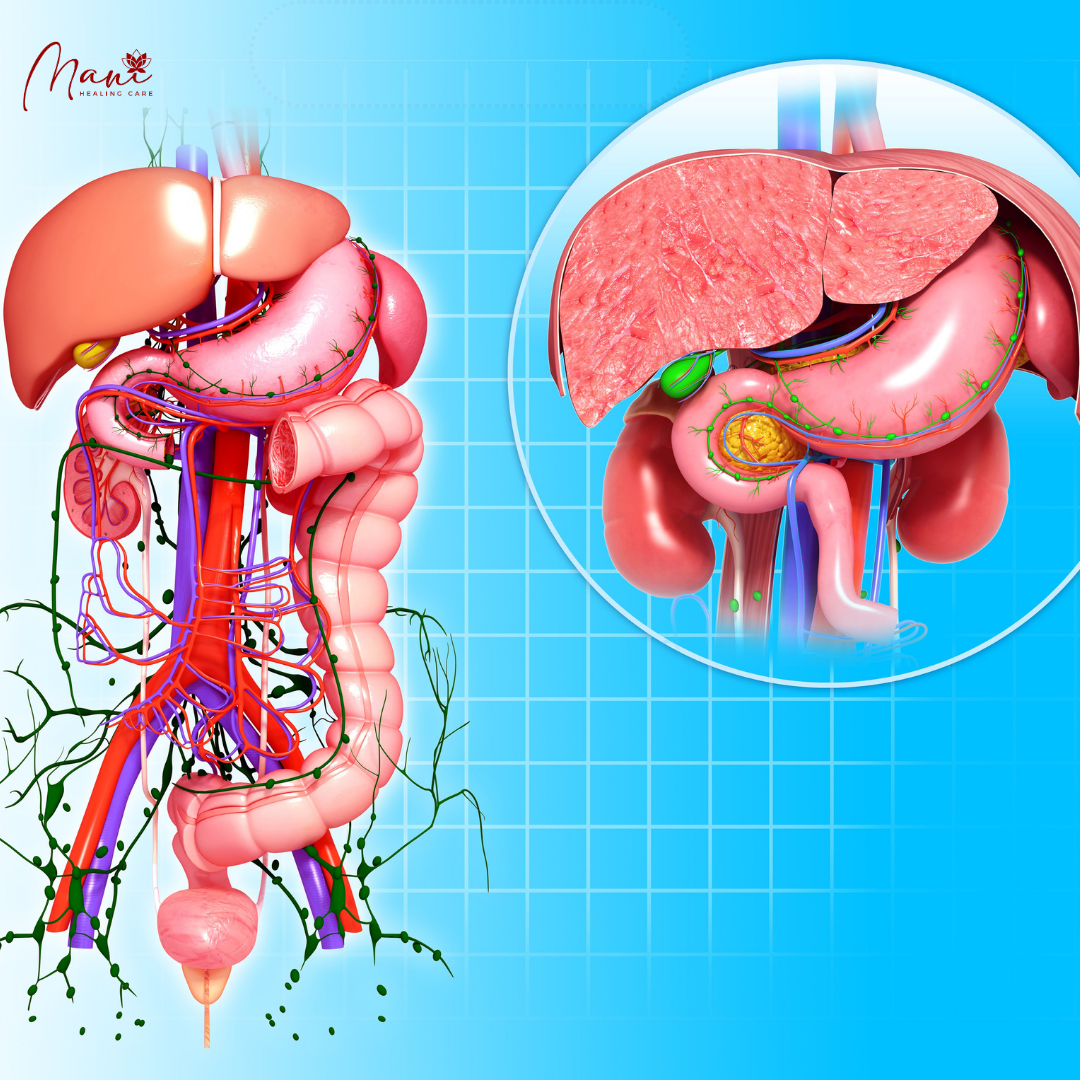
Hệ bạch huyết là một hệ thống phức tạp bao gồm các mạch bạch huyết và các hạch bạch huyết dẫn lưu dịch ngoại bào chứa các mảnh vụn tế bào, nước dư thừa và chất độc vào hệ thống tuần hoàn. Các hạch bạch huyết đóng vai trò như một bộ lọc, do đó, khi dịch bạch huyết quay trở lại tim, nó hoàn toàn vô trùng.
Ngoài ra, hệ thống bạch huyết bao gồm các mô bạch huyết liên quan đến niêm mạc, chẳng hạn như amidan, vòm họng, mảng Peyers ở ruột non và thậm chí cả ruột thừa. Lợi dụng hệ thống thoát nước của bạch huyết, tế bào ung thư xâm nhập vào mạch bạch huyết rồi đến các hạch bạch huyết. Nhìn chung, các hạch bạch huyết có thể đóng vai trò là cửa ngõ trong phần lớn các trường hợp ung thư giai đoạn đầu. Đôi khi, các tế bào ung thư có thể xâm nhập vào mạch máu. Báo cáo này nhấn mạnh tính toàn vẹn cấu trúc của hệ bạch huyết mà qua đó các tế bào ung thư có thể lây lan.
Sử dụng hệ thống mô hình hạch bạch huyết trọng điểm của khối u ác tính và ung thư vú, sự lây lan của ung thư giai đoạn sớm qua hệ thống bạch huyết đang tiến triển trong phần lớn các trường hợp. Hệ thống bạch huyết của các cơ quan nội tạng phức tạp và khó nghiên cứu hơn nhiều. Kiến thức về khối u ác tính và ung thư vú lan đến hạch bạch huyết trọng điểm có thể thiết lập các nguyên tắc cơ bản của di căn ung thư. Mục tiêu của báo cáo này là nhấn mạnh sự phức tạp của hệ bạch huyết. Cho đến nay, các cơ chế phân tử của ung thư lây lan từ vi môi trường ung thư đến hạch bạch huyết và các vị trí ở xa vẫn chưa được hiểu rõ và việc làm sáng tỏ chúng cần được ưu tiên hàng đầu trong nghiên cứu di căn ung thư.
I. Giới thiệu
1 – Nghiên cứu của Stanley P Leong:
Trong thời kỳ chưa có hạch canh gác, người ta cho rằng ung thư sẽ lây lan từ vị trí ban đầu đến các hạch bạch huyết khu vực trước tiên, sau đó đến các vị trí xa hơn. Do đó, Halstad đã thúc đẩy phẫu thuật cắt bỏ vú triệt để bằng phẫu thuật bóc tách toàn bộ hạch nách để điều trị ung thư vú [ 1 ] và Snow đã ủng hộ việc cắt bỏ toàn bộ khối u ác tính nguyên phát cùng với phẫu thuật bóc tách hạch bạch huyết khu vực triệt để [ 2 , 3 ]. Tầm quan trọng của hệ bạch huyết đối với sự di căn của ung thư đã được Haagensen và cộng sự nhấn mạnh và mô tả chi tiết. [ 4 ]. Tác động của Halsted sâu sắc đến mức việc mổ xẻ hạch bạch huyết triệt để đã trở thành tiêu chuẩn cho các loại ung thư khác nhau như ung thư thực quản, dạ dày, đại tràng, phụ khoa và các loại khác.
Mặc dù đã cắt bỏ đầy đủ vị trí ban đầu và bóc tách hạch vùng triệt để, tái phát toàn thân vẫn xảy ra. Vì vậy, Cady khẳng định rằng hạch bạch huyết là điểm đánh dấu chứ không phải là điểm chỉ đạo sự lây lan của ung thư [ 5 ]. Vấn đề khó khăn trong việc đánh giá hạch bạch huyết khu vực nhưng vẫn tránh được việc bóc tách hạch triệt để đã được giải quyết nhờ công trình của Cabanas [ 6 ] sử dụng mô hình dương vật và Morton [ 7 ] sử dụng mô hình khối u ác tính với công trình tiên phong của họ trong việc phát triển trọng điểm Khái niệm hạch bạch huyết (SLN). Các thử nghiệm lâm sàng sau đó về khối u ác tính [ 8 ] và ung thư vú [ 9 ] đã chứng minh rằng sinh thiết SLN là một thủ tục xác định giai đoạn đáng tin cậy cho lưu vực hạch khu vực. Vì vậy, có thể tránh được việc bóc tách hạch triệt để với tỷ lệ mắc bệnh tăng lên nếu sinh thiết SLN âm tính.
Trong kỷ nguyên hậu hạch, chúng ta đã biết rằng, trong hầu hết các trường hợp như khối u ác tính và ung thư vú, ung thư lây lan theo một quá trình có trật tự [ 10 ] từ vị trí ban đầu đến hạch bạch huyết và sau đó xa hơn đến các vị trí xa. Giải phẫu và sinh lý của sự lây lan của ung thư được xác định rõ hơn bằng mô hình lây lan của ung thư nguyên phát sang hạch bạch huyết.
Trong bài viết đánh giá này, chúng tôi muốn xác định rõ hơn về giải phẫu của hệ bạch huyết ở các vị trí giải phẫu được chọn. Alexander Pissas, Muriel Scarato, Francoise Gallon và Marie Helene Pissas mô tả sự dẫn lưu bạch huyết của dạ dày và tuyến tụy dựa trên việc mổ xẻ bằng phẫu thuật và tử thi. Sử dụng các mẫu vật tử thi, Miguel Amore xác định hệ bạch huyết của chi trên và chi dưới tương ứng với nách và háng. Max Wu nghiên cứu hệ bạch huyết và hạch bạch huyết bằng các phương thức hình ảnh khác nhau. Ngoài khối u ác tính, Mark Faries tóm tắt việc áp dụng khái niệm nút trọng điểm và phẫu thuật để đánh giá tình trạng của một số loại ung thư. Amanda Lund theo dõi việc buôn bán tế bào lympho qua các mạch bạch huyết cũng như mối quan hệ giữa các mạch liên quan đến khối u và giám sát miễn dịch. Stanley Leong đưa ra tóm tắt và quan điểm về hệ bạch huyết và SLN liên quan đến di căn ung thư.
II. Dẫn lưu bạch huyết của dạ dày và tuyến tụy: nghiên cứu trên tử thi và người sống
1 – Nghiên cứu của nhóm tác giả: Alexandre Pissas, Muriel Scarato, Francoise Gallon và Marie Helene Pissas
1.1. Dẫn lưu bạch huyết của dạ dày
Rouviere, Cunéo và Delamare đã mô tả ba vùng dẫn lưu của dạ dày: (1) dẫn lưu dạ dày bên trái gần bờ cong nhỏ; (2) hệ thống dẫn lưu lách tương ứng với đáy vị; và (3) dẫn lưu bạch huyết ở gan [ 11 , 12 ]. Khu vực cuối cùng này là mạng lưới lớn nhất và bao gồm phần quan trọng nhất của độ cong lớn hơn và phần hang vị môn vị của dạ dày.
Chúng tôi đã nghiên cứu giải phẫu hệ dẫn lưu bạch huyết của dạ dày và tuyến tụy trong 30 năm qua. Để đánh giá cao hệ thống bạch huyết của các cơ quan tiêu hóa này, chúng tôi đã sử dụng các mẫu vật từ mổ xẻ tử thi và theo dõi sự dẫn lưu bạch huyết của các cơ quan này bằng thuốc nhuộm quan trọng trong quá trình phẫu thuật [ 13 ]. Chúng tôi đã mổ xẻ 20 xác chết không tiêm và 210 xác có tiêm dung dịch Papamiltiades (dầu tuyết tùng màu) và 55 xác chết được tẩm dầu gỗ sứ màu (Hình 2).(Hình.1,1,,2,2,,33Vàvà4).4). Bốn mươi bệnh nhân đã được tiêm Ultra Fluid Lipiodol trong quá trình nội soi xơ hóa và nhuộm màu quan trọng, Pontmine Sky Blue6 BX (Gurr), trong khi phẫu thuật. Những phát hiện của chúng tôi cho thấy vùng lách ít quan trọng hơn vùng dạ dày và gan bên trái, và sự chồng chất của ba vùng này là rất quan trọng. Những phát hiện này cho thấy ung thư có thể lây lan qua hệ bạch huyết ở phần giữa của dạ dày, ở chuỗi dạ dày, lách hoặc gan bên trái. Chúng tôi đã thiết lập sự chồng chất của ba khu vực chính này, trong đó phần giữa của dạ dày chảy qua ống dạ dày, lách hoặc gan bên trái với hướng dẫn lưu bạch huyết theo hướng của các van trên các mạch bạch huyết phụ.




Một đánh giá gần đây về hệ bạch huyết của dạ dày của Lirosi et al. cho thấy hệ thống dẫn lưu bạch huyết của dạ dày rất phức tạp [ 14 ]. Tổng quan nhấn mạnh định hướng giải phẫu phẫu thuật và tuân theo các khuyến nghị của Hiệp hội Nghiên cứu Ung thư dạ dày Nhật Bản [ 15 ].
Các mô hình xác chết có thể thiếu độ chính xác vì các nghiên cứu về xác chết phụ thuộc vào hướng của kim và ống tiêm do nhà giải phẫu thực hiện khi tiêm dầu tuyết tùng có màu. Do đó, các phát hiện về hệ thống bạch huyết trên tử thi cần được bổ sung bằng dòng chảy của thuốc nhuộm quan trọng trong quá trình phẫu thuật. Kết hợp với các tài liệu và các phát hiện trên tử thi và phẫu thuật, chúng tôi có thể kết luận rằng dẫn lưu bạch huyết của dạ dày là nhiều đường dẫn và sự chồng chéo của các đường dẫn này không phải là hiếm như được minh họa trong Hình 2. 5.
1.2. Dẫn lưu bạch huyết của tuyến tụy
Dựa trên việc tiêm tuyến tụy vào tử thi ở 12 người lớn, 15 trẻ sơ sinh chết non và 3 trẻ sơ sinh mắc bệnh Indian Ink, Evans và Ochsner đã tìm thấy hệ thống dẫn lưu lách, tụy dưới, tá tràng trước và sau [ 16 ] mà không nghiên cứu các con đường sau.
Một đánh giá gần đây về hệ bạch huyết của tuyến tụy của Cesmebasi et al. [ 17 ] cho thấy hệ thống bạch huyết tuyến tụy rất phức tạp với một mạng lưới rộng lớn gồm các kênh, mạch bạch huyết và các nút dẫn lưu từ đầu, cổ, thân và đuôi tuyến tụy (Hình 1). 6). Hệ thống bạch huyết phức tạp này của tuyến tụy có mối liên quan trực tiếp với kết quả lâm sàng của viêm tụy và sự lây lan của ung thư tuyến tụy [ 17 ]. Chúng tôi cho rằng hệ thống bạch huyết của tuyến tụy có liên quan đến cơ chế bệnh sinh của viêm tụy cấp tính và mãn tính. Do đó, hệ bạch huyết hoạt động giống như một van an toàn chống lại sự tiến triển của viêm tụy cấp, vì enzyme là các macroprotein và chỉ được hệ bạch huyết hấp thụ.
Các khái niệm của Descomps và Turnesco [ 18 ] đã mang lại sự tiến bộ lớn trong việc nhận biết dẫn lưu bạch huyết vùng bụng – chậu. Rõ ràng là nang nhũ trấp không phải là nguồn gốc của ống ngực nhưng nó đại diện cho một túi giãn dẫn vào ống ngực [ 19 ] (Hình 1). 7). Thân ruột và hai thân thắt lưng chảy vào nang nhũ trấp, là cấu trúc sau phúc mạc và nó nhận dưỡng trấp béo chứa các sản phẩm lipid của quá trình tiêu hóa từ ruột [ 20 ]. Do đó, nang nhũ tương nhận các chất dẫn lưu từ các cơ quan vùng bụng và vùng chậu, hoạt động như một ống dẫn lưu bạch huyết vùng bụng vào ống ngực (Hình 1). số 8).

III. Bạch huyết của nách và háng dựa trên mổ xẻ tử thi
1 – Nghiên cứu của Miguel Amore
1.1.Hạch bạch huyết ở nách
Các hạch bạch huyết ở nách đại diện cho trung tâm dẫn lưu bạch huyết của chi trên và tuyến vú. Chúng tôi đã áp dụng cách phân loại do Caplan đề xuất [ 21 ], liên quan đến dẫn lưu tĩnh mạch của nách, mô tả bốn chuỗi chính sau:
1.2. Chuỗi vú bên
Các nút này được tìm thấy ở gần các mạch nách, trên thành trước của nách và chúng đi theo các mạch vú bên ngoài giữa da vùng trước và sau của ngực. Các mạch đi của nó hướng về phía đỉnh của nách để dẫn bạch huyết vào chuỗi nách và ngực trên, tạo thành nhóm dưới đòn theo tên gọi truyền thống.
1.3. Chuỗi ngực cao cấp
Các hạch này nằm trên thành trong của nách, phía sau cơ ngực và đi theo các mạch máu ngực trên. Các mạch bạch huyết đi của chuỗi này dẫn bạch huyết vào chuỗi tĩnh mạch nách.
1.4. Chuỗi dưới xương vai
Đây là các nút vệ tinh của các mạch dưới xương vai. Chúng nhận được hệ thống dẫn lưu từ thành sau của ngực và với tỷ lệ thấp hơn là dẫn lưu bạch huyết từ thành trước và thành ngực trong (Hình 2).(Hình 9). Dòng chảy ra của chuỗi này hướng đến chuỗi vú ngoài hoặc đến đỉnh của nách, chảy ra ngang mức tĩnh mạch nách.
1.5. Chuỗi tĩnh mạch nách
Chuỗi hạch này nằm ở phần trên của nách, ở gốc đến đỉnh nách ngực. Chuỗi này bao gồm tám đến mười nút cũng như bốn chuỗi phụ: trước, sau, trên và dưới. Chuỗi này nhận được sự dẫn lưu bạch huyết từ tất cả các vùng của chi trên, từ thành trước và thành sau của ngực, cũng như từ phần còn lại của chuỗi dọc của nách. Nói chung, các mạch đi đi theo tĩnh mạch nách để đến góc tĩnh mạch cảnh-dưới đòn của ống ngực [ 22 – 27 ] (Hình 2). 9).
1.6. Con đường bạch huyết phái sinh
Điều quan trọng là phải làm nổi bật sự hiện diện của các đường dẫn bạch huyết của chi trên, đó là những mạch bạch huyết không đến được các hạch bạch huyết ở nách. Chúng bao gồm các mạch máu vùng đầu (Mascagni) [ 26 ], cơ delta-tricipital (Caplan) [ 22 , 26 ] và các mạch máu trong nách (Ciucci) [ 22 , 26 ]. Mặc dù các mạch bạch huyết thay thế này không phải là hệ thống dẫn lưu bạch huyết chính về phía nách nhưng chúng có thể có vai trò rất quan trọng trong việc phục hồi chức năng của bệnh nhân bị phù bạch huyết. Điều quan trọng là phải biết giải phẫu của chúng để có thể bảo tồn chúng [ 22 , 26 ].
Nhận xét giải phẫu và lâm sàng
Đường dẫn lưu bạch huyết chủ yếu từ vú là về phía nách. Bóc tách hạch nách là một phương pháp điều trị phẫu thuật tiêu chuẩn cho những bệnh nhân ung thư vú chọn lọc và cụ thể có hạch dương tính (hạch căng cứng). Thật không may, tỷ lệ phù bạch huyết ở cánh tay là khá thực tế và chắc chắn bị ảnh hưởng bởi phẫu thuật cắt bỏ vì nó được báo cáo ở khoảng 20–30% bệnh nhân được phẫu thuật bóc tách hạch nách [ 28 ]. Hiện nay, sinh thiết hạch bạch huyết (SLN) đã trở thành phương pháp được sử dụng rộng rãi để phẫu thuật xác định giai đoạn hạch nách trong ung thư vú.
Tuy nhiên, để một phẫu thuật ít xâm lấn hơn, tỷ lệ phù bạch huyết ở cánh tay sau sinh thiết SLN là dưới 5% [ 28 ]. Vị trí tối ưu của thuốc nhuộm hoặc tiêm keo vẫn chưa được xác định cho sinh thiết SLN. Các vị trí tiêm thuốc nhuộm trong da, dưới quầng vú, quanh khối u và trong khối u đều đã được báo cáo, mặc dù không có sự đồng thuận nào về vị trí tiêm thuốc nhuộm tối ưu để xác định SLN. Việc xác định vị trí tiêm lý tưởng xuất phát từ kinh nghiệm lâm sàng hơn là từ các nghiên cứu giải phẫu, như Suami et al. đã đề xuất [ 29 ]. Những người tiêm vào vùng dưới quầng vú đều tuân theo khái niệm về đám rối dưới quầng vú được Sappey mô tả vào năm 1874 [ 30 ]. Đám rối này được coi là trung tâm của toàn bộ hệ thống dẫn lưu bạch huyết trong tuyến vú, bất kể khối u có nằm ở bất kỳ phần nào của nó hay không. Nhưng vào năm 1959, Turner-Warwick cho rằng Sappey có thể đã nhầm ống dẫn sữa với mạch bạch huyết vì ông có thể chứng minh sự dẫn lưu thuốc nhuộm hoặc chất đồng vị từ vị trí khối u đến nách mà bỏ qua hoàn toàn đám rối dưới quầng vú [ 31 ]. Công trình nghiên cứu gần đây về dẫn lưu bạch huyết vú ở tử thi cho thấy tiêm gần khối u nguyên phát là cách hiệu quả nhất để xác định SLN [ 29 , 31 ].
1.7. Hạch bẹn
Các hạch này nhận bạch huyết từ chi dưới, cơ quan sinh dục ngoài, rìa hậu môn và thành bụng dưới (Hình 10). Có khoảng 10 hạch trở lên, tất cả đều nằm ở màng nông. Từ thế kỷ XIII đến nay, một số tác giả đã mô tả các hạch bẹn và đề xuất các danh pháp khác nhau để phân loại các nhóm hạch hiện có, nhưng danh pháp đã đứng vững trước thử thách của thời gian là danh pháp do Quènu và Lejars đề xuất [ 32 ]. Họ phân loại các nhóm bằng cách sử dụng hai đường tưởng tượng, một đường vuông góc và một đường thẳng đứng, liên quan đến trục của tĩnh mạch hiển lớn. Sự phân loại này cho phép các nút này được nhóm lại thành bốn nhóm và một nhóm trung tâm [ 22 , 25 ]. Trong nghiên cứu của chúng tôi, chúng tôi đã chia, theo các nhánh vòm của tĩnh mạch hiển lớn, thành ba nhóm trên và hai nhóm dưới: nhóm trên bên ngoài hoặc xương mũ chậu, dưới da bụng giữa hoặc trên, vùng dưới da bên trong hoặc bên ngoài, bên trong hoặc bên trong hiển dưới. và hiển bên ngoài hoặc hiển phụ phía dưới. Các hạch bạch huyết bẹn tốt nhất là dẫn lưu đến hạch bạch huyết Cloquet [ 33 ], nằm dưới dây chằng bẹn và là hạch dưới nhất của chuỗi chậu ngoài. Hạch Cloquet thuộc nhóm trong của chuỗi chậu ngoài [ 30 ]. Các hạch chậu ngoài không được bao gồm trong phân loại này.
IV. Hình ảnh hạch bạch huyết
1 – Nghiên cứu của Max Wu:
Hình ảnh lâm sàng của hạch bạch huyết có thể được chia thành các phương thức giải phẫu và chức năng. Chụp cắt lớp vi tính (CT), siêu âm (US) và chụp cộng hưởng từ (MRI) cung cấp đánh giá giải phẫu hoặc hình thái chi tiết của các hạch bạch huyết, trong khi chụp cắt lớp phát xạ positron (PET) và chụp xạ hình bạch huyết là các kỹ thuật hình ảnh chức năng.
Các hạch bạch huyết bình thường có hình dạng thon dài hoặc hình thận đặc trưng bởi trục dài (dọc theo chiều dài nhất của hạch) và trục ngắn (vuông góc với trục dài). Kích thước hạch bạch huyết được biểu thị bằng kích thước trục ngắn tối đa, phép đo ít biến đổi hơn kích thước trục dài. 10 mm thường được sử dụng làm giới hạn trên của mức bình thường đối với kích thước trục ngắn tối đa đối với các hạch bạch huyết ở trung thất [ 35 ] và ở các vị trí khác (Hình 11). Tất nhiên, các hạch bệnh lý có thể nhỏ hơn 10 mm và các hạch bình thường có thể lớn hơn. Ở các vị trí khác, chẳng hạn như vùng ngực trong (vú trong), các nút thường nhỏ hơn và áp dụng giới hạn kích thước nhỏ hơn. Tiêu chí về kích thước đối với các lưu vực khác có cơ sở bằng chứng hạn chế hơn [ 36 ]. Tiêu chí kích thước trục ngắn 10 mm được chấp nhận rộng rãi và đã được đưa vào Tiêu chí đánh giá đáp ứng ở khối u rắn (RECIST) phiên bản 1.1 [ 37 , 38 ].
CT, siêu âm và MRI thường có thể phân biệt được vỏ hạch với rốn mỡ. Các đặc điểm vi mô nhỏ hơn của hạch bạch huyết, chẳng hạn như nang và trung tâm mầm, không thể được nhìn thấy bằng các phương thức hình ảnh lâm sàng thông thường. Vỏ dày lên hoặc mất rốn mỡ là dấu hiệu bất thường nghi ngờ ác tính (Hình 2). 12), mặc dù điều này cũng có thể chỉ ra nút phản ứng với nhiễm trùng hoặc viêm.
Trong khi các phương thức hình ảnh lâm sàng chủ yếu là giải phẫu cũng có thể cung cấp thông tin chức năng, chẳng hạn như siêu âm Doppler màu về lưu lượng máu và MRI khuếch tán, PET và ghi xạ ảnh bạch huyết là các phương thức chức năng thuần túy thường tương quan với hình ảnh giải phẫu (thường là CT). Đây là các kỹ thuật đánh dấu phóng xạ nhằm phát hiện và khoanh vùng sự tích tụ chất đánh dấu phóng xạ trong các hạch bạch huyết. Chất đánh dấu phóng xạ phổ biến nhất để chụp ảnh PET là flo-18 fluorodeoxyglucose (FDG), một dạng glucose được đánh dấu phóng xạ tích tụ trong các tế bào khối u và các tế bào khác với sự chuyển hóa glucose tăng lên. Các chất đánh dấu phóng xạ PET có bán trên thị trường khác để chụp ảnh khối u bao gồm axit tetraazacyclododecanetetraacetic gallium-68–DPh1-Tyr3-octreotate (DOTATATE), một chất tương tự somatostatin được dán nhãn phóng xạ cho các khối u thần kinh nội tiết [ 39 ] và flo-18 anti-1-amino-3–18F-fluorocyclobutane Axit -1-carboxylic (fluciclovine), một chất tương tự axit amin được dán nhãn phóng xạ cho bệnh ung thư tuyến tiền liệt [ 40 ]. Bất kể chất đánh dấu phóng xạ, các hạch bạch huyết dương tính trên PET đều xuất hiện dưới dạng “điểm nóng” và mối tương quan với CT hoặc MRI cung cấp thông tin định vị và hình thái học (Hình 2). 13AC). Chụp PET các hạch bạch huyết là hữu ích nhất để xác định các hạch di căn trước khi chúng xuất hiện to hơn hoặc bất thường trên hình ảnh giải phẫu.
Trong kỹ thuật xạ hình bạch huyết, chất keo được đánh dấu phóng xạ hoặc tilmanocept technetium-99 m được tiêm trong da với sự hấp thu vào mạch bạch huyết và tích tụ trong các hạch bạch huyết để xác định SLN. Giống như trong PET, các hạch bạch huyết được hình dung là “điểm nóng”. Các mạch bạch huyết cũng có thể được nhìn thấy dưới dạng các cấu trúc tuyến tính hoặc đường cong mờ. Chụp cắt lớp vi tính phát xạ đơn photon (SPECT) cung cấp các hình ảnh cắt ngang có thể được đăng ký cho CT (Hình 2). 14).
Hình ảnh giải phẫu các hạch bạch huyết bằng phương pháp lâm sàng giúp phân biệt bình thường và bất thường dựa trên kích thước và đặc điểm hình thái. Hình ảnh chức năng của các hạch bạch huyết cho thấy các “điểm nóng” phản ánh sự tích tụ tăng lên của glucose được đánh dấu phóng xạ hoặc các phân tử liên kết với thụ thể khác.
V. Ứng dụng phẫu thuật hạch trọng điểm điều trị các loại ung thư
1 – Nghiên cứu của Mark B Faries
Lập bản đồ bạch huyết và sinh thiết hạch bạch huyết (SLN) hiện là thành phần tiêu chuẩn trong điều trị cả khối u ác tính [ 8 ] và ung thư vú [ 9 ]. Đây là sự phát triển tự nhiên vì cả hai loại khối u này đều lan rộng dọc theo đường bạch huyết và di căn hạch mang ý nghĩa tiên lượng quan trọng. Nếu đúng như vậy, thật hợp lý khi hỏi liệu kỹ thuật tương tự có thể áp dụng được cho các loại ung thư khác hay không. Thật vậy, sinh thiết SLN đã được khám phá ở các khối u ác tính khác với mức độ thành công và chấp nhận khác nhau. Trong phần này, cơ sở lý luận của sinh thiết SLN như một khái niệm chung sẽ được xem xét cũng như dữ liệu liên quan đến việc sử dụng nó trong một số khối u ác tính không phải khối u ác tính, không phải ung thư vú (Bảng 11).
Bảng 1: Cơ sở lý luận cho việc lập bản đồ bạch huyết và sinh thiết hạch trọng điểm
| Cơ sở lý luận | Bình luận |
|---|---|
| Cải thiện độ chính xác của nghiên cứu | Các kỹ thuật giải phẫu bệnh chuyên sâu hơn (ví dụ như hóa mô miễn dịch) có thể được áp dụng do số lượng hạch để đánh giá nhỏ hơn nhiều |
| Giảm tỷ lệ mắc bệnh của giai đoạn | Không cần phải mổ xẻ hoàn toàn các nút để có được hầu hết thông tin về giai đoạn |
| Lựa chọn bệnh nhân điều trị toàn bộ lưu vực | Điều này có thể bao gồm phẫu thuật bóc tách hoàn toàn, nhưng cũng có thể liên quan đến bức xạ trong các bệnh nhạy cảm với bức xạ, chẳng hạn như ung thư biểu mô tế bào Merkel. |
| Cải thiện khả năng sống sót nhờ điều trị sớm di căn hạch | Điều này vẫn còn gây tranh cãi và có thể phụ thuộc vào các phần sinh học khối u chưa được hiểu rõ. |
Đầu tiên, tiện ích tiềm năng của khái niệm hạch canh gác là gì? Có một số cách mà sinh thiết hạch bạch huyết (SLN) có thể có giá trị bao gồm tăng độ chính xác của việc xác định giai đoạn, giảm mức độ phẫu thuật và do đó giảm tỷ lệ mắc bệnh.
Phân loại giai đoạn bạch huyết là thành phần trung tâm trong đánh giá tiên lượng của nhiều bệnh ung thư và sự liên quan của các hạch bạch huyết vùng hậu môn thường dẫn đến chỉ định Giai đoạn 3. Tuy nhiên, trong một số trường hợp, độ chính xác của việc xác định giai đoạn bệnh lý có thể không tối ưu ở những bệnh nhân được chỉ định N0 bị tái phát sau đó. Một nguồn tiềm năng của điều này là ở các di căn vi mô bị bỏ sót trong đánh giá bệnh lý tiêu chuẩn. Việc áp dụng các kỹ thuật giải phẫu bệnh chuyên sâu hơn như hóa mô miễn dịch có thể cải thiện độ chính xác của đánh giá bệnh lý, nhưng nhìn chung là không thực tế đối với các mẫu bệnh phẩm bóc tách hạch lớn, hoàn chỉnh [ 41 ]. Tuy nhiên, với sinh thiết hạch bạch huyết (SLN), số lượng hạch bạch huyết cần đánh giá để đưa ra đánh giá bệnh lý chính xác của vùng ít hơn nhiều và các kỹ thuật mô bệnh học toàn diện hơn trở nên khả thi [42 ].
Ngoài việc hỗ trợ đánh giá bệnh lý, sinh thiết hạch bạch huyết (SLN) còn có thể giúp xác định chính xác hơn các hạch bạch huyết liên quan. Việc thoát bạch huyết từ vị trí khối u nguyên phát có thể không thể đoán trước được trong một số trường hợp. Đối với các khối u ác tính ở da, sự dẫn lưu có thể xảy ra ở các vị trí hạch hoặc vị trí ngoài tử cung như vùng biểu mô hoặc vùng khoeo, khoang tam giác giữa các cơ, vùng trong sườn và vùng sau phúc mạc [ 43 ]. Trong các khối u ác tính khác, chẳng hạn như ung thư đại trực tràng, việc dẫn lưu có thể xảy ra ở các vị trí bất thường bên ngoài vị trí mạc treo điển hình dọc theo các mạch nuôi dưỡng [ 44 ]. Sinh thiết hạch bạch huyết (SLN) có khả năng phát hiện các kiểu dẫn lưu bất thường này và xác định vị trí (các) hạch chính xác để đánh giá bệnh lý.
Lý do thứ hai cho sinh thiết hạch bạch huyết (SLN) là để giảm mức độ và do đó giảm tỷ lệ mắc bệnh của điều trị phẫu thuật. Trong khối u ác tính và ung thư vú, điều này là do tránh bóc tách hạch bạch huyết hoàn toàn [ 8 , 45 ]. Lợi ích đặc biệt này có thể bị hạn chế ở một số bệnh, chẳng hạn như ung thư đại trực tràng khi việc mổ xẻ hoàn toàn được thực hiện mà không gây thêm tỷ lệ mắc bệnh đáng kể. Tuy nhiên, trong các loại ung thư khác, chẳng hạn như ung thư dạ dày, có thể việc xác định chính xác mô hình dẫn lưu bằng cách điều chỉnh phẫu tích hạch có thể làm giảm tỷ lệ mắc bệnh [ 46 ].
Cải thiện khả năng sống sót là mục tiêu bổ sung của sinh thiết SLN và phẫu thuật hạch vùng. Chủ đề này gây nhiều tranh cãi hơn và cuộc thảo luận đầy đủ về bằng chứng ủng hộ và chống lại tác động sinh tồn sẽ được dành cho một địa điểm khác.
2 – Các khối u ác tính ở da không phải hắc tố
Các bệnh ung thư da khác có nguy cơ di căn hạch thực sự, bao gồm ung thư biểu mô tế bào Merkel và ung thư biểu mô tế bào vảy ở da. Ung thư biểu mô tế bào Merkel là một chẩn đoán không phổ biến, nhưng khi nó xuất hiện các hạch bạch huyết là vị trí di căn ban đầu phổ biến nhất [ 47 ], sinh thiết SLN đã được sử dụng thành công trong việc xác định giai đoạn các hạch bạch huyết khu vực. Các đặc điểm của tế bào Merkel bao gồm đường kính và độ sâu của khối u nguyên phát có liên quan đến nguy cơ liên quan đến hạch, với các khối u lớn hơn có nguy cơ cao hơn [ 48 ]. Tuy nhiên, chưa có phân nhóm nào được xác định có nguy cơ liên quan đến hạch dưới 10% và các hướng dẫn hiện tại khuyến nghị xem xét sinh thiết SLN trong mọi trường hợp ở những bệnh nhân có chỉ định phẫu thuật. Ý nghĩa tiên lượng của SLN dương tính trong tế bào Merkel không đáng kể như trong khối u ác tính. Điều này một phần là do tuổi cao và bệnh đi kèm ở nhiều bệnh nhân mắc bệnh tế bào Merkel dẫn đến tăng nguy cơ tử vong do các nguyên nhân khác. Có vẻ như di căn SLN có liên quan đến nguy cơ di căn xa cao hơn [ 49 ]. Tuy nhiên, lợi ích chính của sinh thiết SLN trong tế bào Merkel có thể là trong việc lựa chọn những bệnh nhân cần được xạ trị đến các hạch bạch huyết vùng hậu môn. Trong hầu hết các trường hợp, việc dự trữ bức xạ vào khu vực đó có vẻ an toàn đối với những bệnh nhân có SLN âm tính. Đối với những người có di căn SLN, bức xạ không bóc tách dường như mang lại khả năng kiểm soát bệnh khu vực tốt [ 50 ].
Ung thư biểu mô vảy ở da là một chẩn đoán cực kỳ phổ biến và phần lớn các bệnh ung thư này không lan đến các hạch bạch huyết. Tuy nhiên, ngay cả một thiểu số nhỏ của bệnh ác tính phổ biến như vậy đại diện cho một số lượng lớn các trường hợp tuyệt đối và đã có mối quan tâm đáng kể trong việc xác định một nhóm bệnh nhân có “nguy cơ cao” liên quan đến hạch và những người nên tiến hành sinh thiết SLN. Một số hệ thống phân giai đoạn hiện đang được sử dụng bao gồm Phiên bản thứ 8 của Hệ thống phân giai đoạn của Ủy ban hỗn hợp Hoa Kỳ về ung thư và hệ thống phân giai đoạn của Brigham và Phụ nữ. Các hệ thống này dường như xác định được những bệnh nhân có nguy cơ tái phát và di căn cao hơn, nhưng không rõ liệu họ có thể chọn bệnh nhân để sinh thiết SLN hay không. Nghiên cứu bổ sung trong lĩnh vực này sẽ hữu ích để xác định bệnh nhân nào có nhiều khả năng được hưởng lợi nhất từ thủ thuật này.
Di căn bạch huyết từ ung thư đại trực tràng cũng là một con đường lây lan phổ biến. Mặc dù bóc tách toàn bộ hệ bạch huyết là một phần tiêu chuẩn của bất kỳ phương pháp cắt bỏ đại tràng nào đối với bệnh ung thư, việc lập bản đồ bạch huyết có thể mang lại hai lợi ích. Đầu tiên, sự dẫn lưu bất thường đến một vị trí nút bên ngoài khu vực mổ tiêu chuẩn đã được xác định lên đến 10% trường hợp [ 44 ]. Lập bản đồ bạch huyết có thể xác định các nút thường bị bỏ qua. Thứ hai, phân tích chuyên sâu hơn về một số lượng nhỏ SLN có thể cải thiện việc dàn dựng. Điều này có thể xác định thêm các bệnh nhân ở giai đoạn III, nhưng quan trọng hơn là nó có thể cho phép những bệnh nhân thực sự âm tính với hạch tránh được hóa trị [ 51 ]. Tuy nhiên, bên ngoài một số trung tâm chuyên khoa, việc lập bản đồ chính xác về ung thư ruột kết là một thách thức và kỹ thuật này vẫn đang được nghiên cứu ở hầu hết các địa điểm.
Phẫu tích hạch trong ung thư dạ dày là nguồn gây tranh cãi đáng kể trên toàn thế giới. Ở châu Á, nơi có tỷ lệ ung thư dạ dày đặc biệt cao, đã có những tiến bộ đáng kể trong việc giảm tỷ lệ mắc bệnh và mức độ phẫu thuật cho những bệnh nhân mắc bệnh ở giai đoạn đầu. Lập bản đồ bạch huyết đã được đưa vào tiến trình này, đặc biệt là ở Nhật Bản [ 46 , 52 , 53 ] như đã đề cập trước đó. Việc sử dụng các thiết bị đánh dấu huỳnh quang cho phép lập bản đồ trong bối cảnh các thủ thuật nội soi và robot với việc bóc tách hạch phù hợp với mô hình dẫn lưu của từng khối u nguyên phát. Điều này hứa hẹn sẽ cải thiện khả năng phục hồi và chất lượng cuộc sống trong khi vẫn duy trì việc phân giai đoạn và điều trị chính xác và đầy đủ.
Ung thư phổi là một trong những bệnh ác tính phổ biến nhất và nguy hiểm nhất, nhiều bệnh nhân bị tái phát mặc dù giai đoạn hạch âm tính tại thời điểm phẫu thuật. Đánh giá kỹ lưỡng hơn các hạch bạch huyết phổi có liên quan đến việc cải thiện giai đoạn và kết quả [ 54 ]. Việc áp dụng bản đồ bạch huyết vào bệnh ung thư phổi đặc biệt khó khăn do không gian hạn chế về mặt vật lý của khoang ngực với các hạch thường ở gần khối u nguyên phát. Việc lập bản đồ bằng thuốc nhuộm màu xanh quan trọng cũng khó khăn hơn do tính chất anthracotic của các hạch bạch huyết phổi. Loạt sản phẩm gần đây sử dụng thuốc nhuộm huỳnh quang và hình ảnh cận hồng ngoại đã chứng minh khả năng sống sót vượt trội ở những bệnh nhân được xác định là không có di căn hạch thông qua sinh thiết SLN [ 55 ].
Việc xác định giai đoạn hạch bạch huyết cũng rất quan trọng trong các khối u ác tính phụ khoa và bóc tách hạch là một phần điều trị tiêu chuẩn cho nhiều bệnh nhân ung thư buồng trứng, cổ tử cung và tử cung. Tuy nhiên, lập bản đồ bạch huyết và sinh thiết SLN chưa được áp dụng rộng rãi. Nghiên cứu tiếp tục xác định vai trò của sinh thiết SLN đối với những bệnh đó. Trong bệnh ung thư buồng trứng, các nút Sentinel trong nghiên cứu Thử nghiệm ung thư buồng trứng giai đoạn đầu (SELLY) đã sử dụng phương pháp lập bản đồ bằng cách tiêm indocyanine green vào cuống buồng trứng với tỷ lệ phát hiện SLN là 68% và độ nhạy cao [ 56 ]. Trong ung thư cổ tử cung, một phân tích tổng hợp gần đây bao gồm 21 nghiên cứu và 2234 bệnh nhân đã tìm thấy bản đồ bạch huyết với độ nhạy đặc hiệu theo từng bên là 88%. Tỷ lệ phát hiện cụ thể của từng bên tương tự với phương pháp lập bản đồ dựa trên technetium hoặc indocyanine dựa trên màu xanh lá cây [ 57 ]. Trong ung thư nội mạc tử cung, so sánh hồi cứu sinh thiết SLN với bóc tách hạch hoàn chỉnh cho thấy ít biến chứng hơn đối với bệnh nhân SLN, đặc biệt liên quan đến phù bạch huyết [ 58 ]. Các so sánh hồi cứu tương tự cho thấy kết quả ung thư tương đương hoặc được cải thiện, mặc dù việc đánh giá thử nghiệm lâm sàng trong tương lai cho câu hỏi này vẫn còn thiếu [ 59 ].
Cuối cùng, ung thư tiết niệu là một trong những lĩnh vực được quan tâm sớm nhất trong khái niệm SLN [ 6 ]. Trong ung thư dương vật, các hướng dẫn hiện hành cho phép sinh thiết SLN như một phương pháp thay thế cho bóc tách bẹn ở bệnh giai đoạn đầu, nhưng trong ung thư tuyến tiền liệt, kỹ thuật này vẫn chưa được chấp nhận rộng rãi [ 60 ]. Sự đổi mới công nghệ, đặc biệt là về máy theo dõi và hình ảnh, hứa hẹn sẽ làm cho kỹ thuật này trở nên chính xác và hữu ích hơn trong căn bệnh đó [ 61 ].
Nhìn chung, rõ ràng là quy trình lập bản đồ dẫn lưu bạch huyết của vị trí khối u nguyên phát và đánh giá (các) SLN trực tiếp trên các con đường đó cung cấp một bức tranh có độ chính xác cao về việc liệu các khối u có bắt đầu lan rộng qua con đường đó hay không. Giá trị của thủ tục này vượt ra ngoài khối u ác tính và ung thư vú, nơi nó đã trở thành một tiêu chuẩn được thiết lập tốt. Tuy nhiên, giá trị của việc áp dụng kỹ thuật này cho các khối u ác tính khác sẽ phụ thuộc vào đặc điểm sinh học của loại khối u đó, tức là liệu khối u có lây lan chủ yếu đến các hạch bạch huyết khu vực theo phương thức đầu tiên hay nguyên phát hay không và những thách thức kỹ thuật về vị trí giải phẫu của khối u. Những yếu tố này, cùng với sự làm việc chăm chỉ của các bác sĩ phẫu thuật trong nghiên cứu lâm sàng, sẽ quyết định tốc độ và bao xa mà sinh thiết SLN sẽ mở rộng phạm vi lấy mẫu ung thư trong ung thư thực quản và dạ dày.
VI. Mạch bạch huyết liên quan đến khối u và giám sát miễn dịch
1 – Nghiên cứu của Amanda W. Lund
Mặc dù người ta chú ý nhiều đến sự góp phần của mạch bạch huyết vào sự di căn của khối u ác tính, điều quan trọng cần nhớ là sự vận chuyển bạch huyết hướng tâm ở trạng thái ổn định là rất quan trọng để giám sát miễn dịch [ 62 , 63 ]. Bạch huyết vận chuyển các kháng nguyên và tế bào đuôi gai (DC) từ các mô không phải bạch huyết ngoại biên đến các hạch bạch huyết nơi tương tác với các tế bào lympho ngây thơ sẽ kích hoạt các phản ứng miễn dịch thích ứng. Bằng chứng ban đầu về tầm quan trọng của việc vận chuyển bạch huyết trong giám sát miễn dịch ở khối u ác tính đến từ các nghiên cứu trên chuột, trong đó yếu tố tăng trưởng mạch bạch huyết, yếu tố tăng trưởng nội mô mạch máu (VEGF-C), được biểu hiện quá mức trong các tế bào khối u ác tính và được cấy vào vật chủ có khả năng miễn dịch [ 64 ]. Trong khi nghiên cứu trước đây đã chứng minh mối liên hệ rõ ràng giữa sự biểu hiện quá mức của VEGF-C, sự hình thành mạch bạch huyết và sự di căn hạch [ 65 , 66 ], việc sử dụng động vật bị suy giảm miễn dịch trong các thí nghiệm này đã làm mất đi cơ hội điều tra các tác động về mặt miễn dịch. Trong khi sự biểu hiện quá mức của VEGF-C ở các vật chủ có khả năng miễn dịch vẫn có khả năng di căn, thì bằng chứng rõ ràng hơn là sự hình thành mạch bạch huyết liên quan đến khối u đã thúc đẩy sự vận chuyển chất lỏng và DC đến các hạch bạch huyết và tình trạng viêm trong khối u [ 64 ] dẫn đến giả thuyết rằng vận chuyển bạch huyết không chỉ cần thiết cho hệ miễn dịch. giám sát nhưng có thể được tăng cường vì lợi ích điều trị. Hai nghiên cứu bổ sung điều tra sự phát triển của khối u ác tính [ 63 ] và sự khởi đầu [ 67 ] ở những con chuột thiếu mạch bạch huyết ở da đã ủng hộ giả thuyết này, theo đó việc thiếu mạch bạch huyết ở da và sự vận chuyển bạch huyết hướng tâm liên quan làm giảm đáng kể tình trạng viêm liên quan đến khối u, tỷ lệ khởi đầu và di căn của khối u và làm suy yếu việc tạo ra các phản ứng tế bào T CD8 + gây độc tế bào de novo. Mối liên quan tiền lâm sàng giữa mạch bạch huyết và tình trạng viêm liên quan đến khối u đã được khám phá ở một mức độ nào đó trên bệnh nhân [ 63 , 68 , 69 ], nhưng vẫn còn nhiều việc phải làm để hiểu mức độ mà bản thân mật độ mạch bạch huyết là đại diện cho khối u. – viêm liên quan trong mẫu bệnh nhân.
Dựa trên sự thay đổi mô hình này, nghiên cứu gần đây đã áp dụng phương pháp trị liệu để hỏi xem liệu sự biểu hiện quá mức của VEGF-C có thể cải thiện khả năng đáp ứng với liệu pháp miễn dịch tiền lâm sàng hay không. Trong cả hai mô hình u ác tính ở chuột [ 68 ] và u nguyên bào thần kinh đệm [ 70 ], các khối u do viêm do VEGF-C gây ra đã phản ứng với việc phong tỏa điểm kiểm soát miễn dịch và tạo ra các phản ứng đặc hiệu với kháng nguyên lâu dài giúp thiết lập trí nhớ có khả năng giảm tái phát. Giả định từ công trình này là sự vận chuyển bạch huyết tăng cao và sự di chuyển DC đến các hạch bạch huyết giúp tăng cường sự hiện diện của các kháng nguyên liên quan đến khối u đến hạch bạch huyết. Tuy nhiên, do vai trò được ghi nhận rõ ràng của VEGF-C trong việc thúc đẩy sự di căn và các cơ chế chồng chéo được sử dụng bởi DC và tế bào khối u để tiếp cận các mạch bạch huyết hướng tâm [ 71 – 73 ], sự an toàn của phương pháp điều trị hỗ trợ tạo lympho ở bệnh nhân vẫn còn là vấn đề cần quan tâm. xác định (Hình. 15).

Điều quan trọng là, tác dụng tích cực của liệu pháp miễn dịch trong bối cảnh tăng sinh mạch bạch huyết có thể bị giảm bớt do các hiện tượng ức chế miễn dịch ở các hạch bạch huyết dẫn lưu khối u [ 74 ], có thể là kết quả của các yếu tố được truyền qua bạch huyết. Đến thời điểm này, sự biểu hiện quá mức của VEGF-C trong khối u ác tính thực sự ngăn chặn sự hình thành mồi mới của tế bào T CD8 + đặc biệt trong các hạch bạch huyết dẫn lưu khối u, ít nhất một phần là do khả năng nhặt rác và trình diện chéo độc đáo của các tế bào nội mô bạch huyết [ 64 , 75 ]. Ngoài ra, các mao mạch bạch huyết ngoại vi và các hạch bạch huyết tương ứng của chúng biểu hiện các điểm kiểm soát miễn dịch ức chế và có thể trực tiếp làm suy giảm các phản ứng miễn dịch chống khối u [ 76 – 78 ]. Do đó, mạch bạch huyết chứa nhiều cơ chế chồng chéo có khả năng hội tụ theo cách đặc hiệu của mô để điều chỉnh khả năng miễn dịch chống khối u.
Cuối cùng, mặc dù nhiều sự chú ý hướng vào DC với tư cách là trung gian trung gian quan trọng trong giám sát miễn dịch, các tế bào lympho T cũng có rất nhiều trong bạch huyết và động lực của việc chúng đi vào và ra khỏi khối u phần lớn vẫn chưa được khám phá. Thông qua việc sử dụng chuyển đổi quang học in vivo, các nghiên cứu gần đây chỉ ra rằng các tế bào T CD8 + , CD4 + và gamma delta tiếp cận các mạch bạch huyết liên quan đến khối u để thoát ra khỏi môi trường vi mô khối u [ 79 , 80 ]. Các tế bào T CD8 + tác động mới được thải ra gần đây vẫn duy trì khả năng sản xuất các cytokine gây độc tế bào để đáp ứng với sự kích thích ex vivo [ 80 ] và có thể đại diện cho một nhóm tế bào T gây độc tế bào có khả năng tiêu diệt khối u có liên quan đến mặt trị liệu. Mặc dù cả hậu quả chức năng của sự thoát ra của tế bào T và các cơ chế điều chỉnh nó vẫn chưa rõ ràng, nhưng việc tiếp tục nghiên cứu trong lĩnh vực này có thể tiết lộ các điểm kiểm soát mới đối với việc điều khiển các phản ứng miễn dịch tại chỗ, tác động vì lợi ích của bệnh nhân. Khi ý nghĩa miễn dịch của việc vận chuyển bạch huyết hướng tâm và quá trình tạo mạch bạch huyết tiếp tục xuất hiện, công việc trong tương lai sẽ cần phải đánh giá cẩn thận các tác động tương đối của quá trình tạo mạch bạch huyết đối với khả năng miễn dịch và di căn để đưa ra các chiến lược điều trị an toàn và hiệu quả cho ứng dụng trong tương lai.
VII. Tóm tắt và triển vọng tương lai
1 – Nghiên cứu của Stanley P. Leong
Đối với bài viết đánh giá này, cơ sở giải phẫu của hệ bạch huyết ở các vị trí khác nhau được tóm tắt bởi Alex Pissas et al. liên quan đến hệ bạch huyết của dạ dày và tuyến tụy và của Miguel Amore cho chi trên và chi dưới. Max Wu mô tả hình ảnh của hệ bạch huyết và các hạch bạch huyết. Hơn nữa, Mark Faries đề cập đến khái niệm SLN lần đầu tiên được giới thiệu trong khối u ác tính và sau đó áp dụng cho các loại ung thư khác. Ngoài mô tả giải phẫu và vai trò sinh lý của hệ bạch huyết bao gồm SLN, Amanda Lund còn thảo luận về mối liên hệ phân tử giữa khối u và mạch bạch huyết cho thấy vai trò quan trọng của việc giám sát miễn dịch khối u bằng hệ bạch huyết. Trong khi các mạch bạch huyết tạo điều kiện thuận lợi cho di căn khu vực, chúng cũng đóng một vai trò quan trọng trong việc giám sát miễn dịch. Định nghĩa tốt hơn về cơ chế phân tử vận chuyển bạch huyết có thể chỉ ra các chiến lược mới để ngăn chặn sự di căn của ung thư đồng thời thúc đẩy khả năng miễn dịch chống khối u.
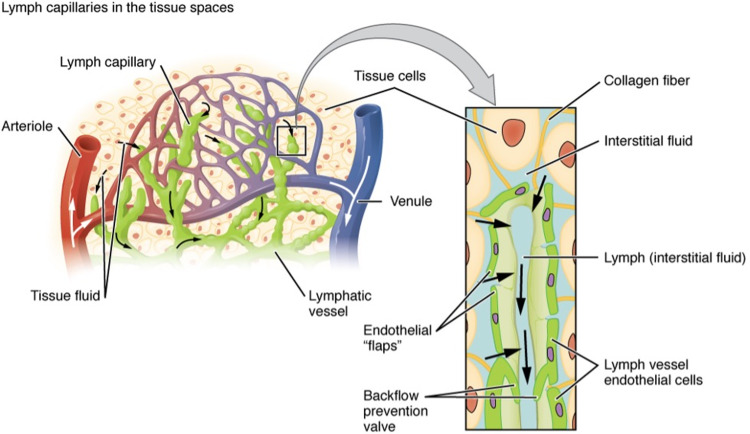
Hệ thống bạch huyết bao gồm các mạch bạch huyết và các hạch bạch huyết và đóng một vai trò sinh lý quan trọng trong hệ thống tuần hoàn của cơ thể như một hệ thống thoát nước chính để đưa khoảng 3 trong số 20 L chất lỏng (10–15%) từ không gian kẽ hàng ngày, chứa các chất thải bao gồm mảnh vụn tế bào, đại phân tử protein, nước dư thừa và chất độc (Hình 2).(Hình 8)số 8) [ 81 ]. Ngoài ra, hệ bạch huyết còn bao gồm các mô bạch huyết liên quan đến niêm mạc như amidan, vòm họng, mảng Peyer ở ruột non và thậm chí cả ruột thừa. Đường kính trung bình của mạch bạch huyết là 100 micron với các van bán nguyệt một chiều. Các mạch bạch huyết có thành mỏng và thành được lót bởi các tế bào nội mô được bao quanh bởi các cơ trơn với lớp ngoài cùng là lớp vỏ giúp neo các mạch bạch huyết vào mô xung quanh, chủ yếu là mô mỡ [ 82 ]. Nhân vật 16hiển thị bản vẽ chi tiết để minh họa giải phẫu vi mô của cấu trúc mạch bạch huyết [ 83 ]. Một số dấu hiệu phân tử đã được tìm thấy và mô tả ở các tế bào nội mô bạch huyết nhưng không có ở các tế bào nội mô máu. Do đó, việc xác định các mạch bạch huyết đã được thực hiện dễ dàng bằng phương pháp dán nhãn miễn dịch huỳnh quang hoặc hóa mô miễn dịch. Các dấu hiệu phân tử này bao gồm gen thịnh vượng của Drosophila melanogaster homeobox, được gọi là thịnh vượng homeobox protein 1 (PROX1 hoặc Prox1; viết tắt tương ứng cho protein của người và động vật gặm nhấm), thụ thể hyaluronan 1 của tế bào nội mô mạch bạch huyết (LYVE1 hoặc Lyve1), tăng trưởng nội mô mạch máu yếu tố thụ thể-3 (VEGFR3) và podoplanin. Những dấu hiệu này đã được chứng minh là hữu ích để xác định các mạch bạch huyết thường được sử dụng kết hợp với nhau hoặc với một dấu hiệu nội mô [ 82 ]. Các mạch bạch huyết chảy vào các hạch bạch huyết, nhà máy sản xuất các tế bào miễn dịch như tế bào T, tế bào B, tế bào đuôi gai và đại thực bào. Có khoảng 600 hạch bạch huyết trong cơ thể trong hệ thống bạch huyết. Vai trò sinh lý chính của hệ bạch huyết là lọc các chất thải của cơ thể và chống nhiễm trùng thông qua khả năng miễn dịch bẩm sinh và đặc hiệu. Để xem xét chi tiết hơn về giải phẫu và sinh lý của hệ bạch huyết, thông tin bổ sung có sẵn trong các đánh giá riêng biệt [ 83 – 85 ].
Các tế bào ung thư khai thác hệ thống bạch huyết như một đường dẫn để di chuyển từ vị trí ban đầu từ môi trường vi mô của chúng và xâm nhập vào các mạch bạch huyết hướng tới các hạch bạch huyết và xa hơn đến các vị trí ở xa. Đường kính trung bình của tế bào lympho là 15 micron và đường kính trung bình của tế bào ung thư lớn hơn tế bào lympho một chút, lên tới 20 micron trở lên. Kích thước của một tế bào ung thư có thể di chuyển thoải mái trong mạch bạch huyết 100 micron. Người ta đã chứng minh rằng các mạch bạch huyết do ung thư gây ra bằng quá trình tạo mạch bạch huyết có thể bị giãn ra [ 86 ]. Người ta suy đoán rằng một cụm tế bào ung thư có thể bị tắc nghẽn trong mạch bạch huyết ở van mạch bạch huyết [ 87 ] và cuối cùng phát triển trên thành trong của mạch bạch huyết dưới dạng khuẩn lạc để phát triển vào mô mỡ xung quanh khi di chuyển di căn, chẳng hạn như trường hợp u ác tính. Người ta cũng có thể suy đoán rằng các tế bào ung thư có thể có một thụ thể đặc hiệu để gắn vào mặt trong của mạch bạch huyết và thiết lập nơi cư trú.
Bài viết đánh giá này mô tả cơ sở giải phẫu của hệ thống bạch huyết ở người với sự nhấn mạnh đến các con đường lây lan ung thư tiềm tàng qua hệ thống bạch huyết. Trong một bài viết đánh giá riêng biệt, các cơ chế phân tử của sự di căn của ung thư qua bạch huyết so với mạch máu sẽ được thảo luận chi tiết với sự nhấn mạnh vào quá trình tạo mạch bạch huyết do ung thư [ 88 ]. Rõ ràng từ các phần riêng lẻ của bài viết đánh giá này là hệ bạch huyết dẫn lưu các cơ quan khác nhau trong cơ thể không đồng nhất, với các kênh bạch huyết dẫn lưu các cơ quan nội tạng phức tạp hơn (Hình 2). số 8) so với các vùng ngoại vi như da và vú. Dẫn lưu SLN cho khối u ác tính và ung thư vú đi theo các con đường đáng tin cậy hơn so với các cơ quan nội tạng như phổi, dạ dày, tuyến tụy và các cơ quan khác, vốn có mô hình dẫn lưu bạch huyết phức tạp. Chắc chắn, khối u ác tính và ung thư vú cho phép chúng ta đánh giá cao đặc điểm sinh học của bệnh ung thư sớm đến SLN với gánh nặng khối u tối thiểu. Người ta đã chứng minh rằng bệnh nhân u ác tính có sinh thiết SLN âm tính có tỷ lệ tái phát thấp từ 5–10% [ 89 , 90 ]. Đối với bệnh nhân ung thư vú có sinh thiết SLN âm tính, tỷ lệ tái phát cũng rất thấp, dưới 5% [ 91 ]. Nhìn chung, bệnh nhân u ác tính hoặc ung thư vú có kết quả sinh thiết SLN âm tính tốt hơn nhiều so với những bệnh nhân có sinh thiết SLN dương tính [ 92 , 93 ]. Vì vậy, điều quan trọng là phải tìm hiểu sinh học về buôn bán ung thư và di căn hạch trong khối u ác tính sớm và ung thư vú để đánh giá cao cơ chế lây lan của ung thư từ vị trí ban đầu đến các hạch bạch huyết và xa hơn đến các vị trí xa. Liệu có những con đường lây lan riêng biệt từ vị trí ban đầu qua các mạch máu ngoài hệ thống bạch huyết hay không sẽ được đề cập đầy đủ trong hai bài báo đánh giá [ 88 , 94 ]. Tính đơn giản tương đối của sự di căn của khối u ác tính và ung thư vú thông qua SLN, trái ngược với hệ thống bạch huyết phức tạp của dạ dày, tuyến tụy và các cơ quan khác, giống như khám phá của Mendel về sự phân chia độc lập của các alen di truyền trội và lặn trong mô hình hạt đậu với về bảy đặc điểm của đậu Hà Lan bao gồm cao và ngắn, nhẵn và nhăn, xanh và vàng và các đặc điểm khác [ 95 ]. Nếu Mendel sử dụng các biến thể màu tóc của con người để nghiên cứu mô hình di truyền về di truyền, thì ông ấy đã không đi đến những kết luận rõ ràng và rời rạc này vì có nhiều gen chéo liên quan đến di truyền màu tóc. Do đó, mô hình SLN cho khối u ác tính và ung thư vú, tương đối đơn giản, sẽ giúp chúng ta hiểu được sự lây lan của ung thư đến hạch bạch huyết và sự tương tác của nó trong các kênh bạch huyết. Môi trường vi mô bên trong vị trí khối u nguyên phát và SLN liên quan đến sự phát triển và lan rộng của ung thư đang chờ nghiên cứu thêm [ 96 ].
Có thể bạn quan tâm:
-
Bệnh tự kỷ, giảm trí nhớ và sương mù não: Thải độc Hệ bạch huyết vùng đầu như thế nào?
-
Hệ thống bạch huyết: Đánh giá về tác động của nắn chỉnh xương
-
Lập bản đồ hệ thống bạch huyết trên các quy mô cơ thể và các lĩnh vực chuyên môn: Báo cáo từ hội thảo của Viện Tim, Phổi và Máu Quốc gia năm 2021 tại Hội nghị chuyên đề về bạch huyết Boston
-
Cấu trúc và sinh lý mạng lưới mạch bạch huyết – Phần 8: Bạch huyết đường liêu hóa và liệu pháp miễn dịch
-
Cấu trúc và sinh lý mạng lưới mạch bạch huyết – Phần 7: Phù bạch huyết